4 Voraussetzungen für den Verkauf in Europa und Großbritannien
CPSR: Bevor wir zum Kern der Sache kommen, ist es immer gut, sich daran zu erinnern, was nötig ist, um ein kosmetisches Produkt in Europa und Großbritannien zu verkaufen. Wie wir bereits in unserem Artikel “So erreichen Sie die EU-Konformität in drei Schritten” erwähnt haben , müssen Sie über die folgenden 4 Elemente verfügen:
- CPSR(Cosmetic Product Safety Report) & Produktinformationsdatei(PIF). Für eine ausführliche Erklärung lesen Sie bitte unseren Artikel hier;
- Ein vorschriftsmäßiges Etikett und seine Angaben;
- Meldung an das europäische Portal CPNP und an das britische Portal SCPN, wenn Sie beabsichtigen, Ihre Produkte auch in das Vereinigte Königreich zu exportieren und dort zu verkaufen;
- Das letzte Element ist die gesetzliche Vertretung, d.h. die verantwortliche Person mit Sitz in der EU und im Vereinigten Königreich, wenn Ihre kosmetischen Produkte auch im Vereinigten Königreich erhältlich sind.
Wenn eine Kosmetikmarke, die in Europa und im Vereinigten Königreich verkaufen möchte, eine der 4 oben genannten Voraussetzungen nicht erfüllt, können wir zweifellos sagen, dass der Handel nicht möglich ist: Kein Markt / Unerlaubter Markt / Kein autorisierter Handel / Pas de Marché / kein Markt / Ningún Mercado / ノーマーケット.
Vergessen Sie nicht, dass Biorius Sie bei diesem Prozess von Anfang bis Ende unterstützen kann. Weitere Informationen über die 5 Schritte und die Expertise von BIORIUS zur EU-Verordnung finden Sie hier.
Erläuterung zum Bericht über die Sicherheit kosmetischer Mittel (CPSR)
Dieser Artikel soll für mehr Klarheit und zusätzliche Informationen über den Cosmetic Product Safety Report(CPSR) sorgen. Im Englischen wird CPSR auch häufig als‘Safety Assessment‘ bezeichnet.

Wo können wir den CPSR finden?
Zunächst einmal ist es wichtig zu wissen, dass dieses Dokument im PIF eines jeden kosmetischen Produkts zu finden ist. Vergessen Sie nicht, dass die Produktinformationsdatei in der Praxis ein elektronischer Ordner ist, der aus mehreren Unterordnern besteht, die Dateien, in der Regel PDFs, enthalten, darunter auch den CPSR.
Die Bedeutung des CPSR und die Inspektion der nationalen Behörden
Man könnte sogar sagen, dass der CPSR der wichtigste Bericht ist, wenn es darum geht, ein Kosmetikprodukt auf dem europäischen und britischen Markt zu platzieren. Allerdings wollen wir die Bedeutung der anderen Dokumente des PIF nicht schmälern. Das Etikett und die konforme Formel, die Meldungen an die Portale und die verantwortliche Person sind ebenfalls wesentliche Elemente für die vollständige Einhaltung der europäischen und britischen Vorschriften.
Darüber hinaus ist der CPSR zweifellos das Dokument, das von den zuständigen nationalen Behörden am häufigsten geprüft wird. Wenn also keine Spur des CPSR im PIF zu finden ist oder Sie bei der Erstellung des CPSR nachlässig waren, ist das ein Grund, warum Sie sich nicht darum kümmern sollten, kann dies zu sehr hohen Geldstrafen, einem sofortigen Rücktritt und einer Meldung an RAPEX führen. Für diejenigen, die es noch nicht wissen: RAPEX ist das Überwachungssystem der nationalen EU-Behörden. Sobald Ihre Kosmetikmarke bei RAPEX erwähnt wird, können Sie eine systematische und sorgfältige Prüfung aller Ihrer Produkte erwarten…
Welche Art von Informationen muss der CPSR enthalten?
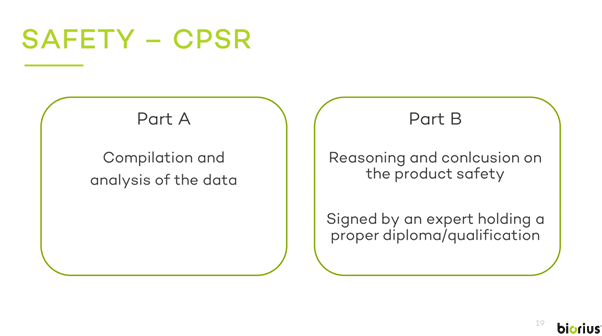
In der Praxis besteht der CPSR aus zwei Teilen, TEIL A und TEIL B: die Anhang I von VERORDNUNG (EG) Nr. 1223/2009 DES EUROPÄISCHEN PARLAMENTS UND DES RATES vom 30. November 2009 über kosmetische Mittel nennt eindeutig alle Informationen, die der Sicherheitsbewerter sammeln und verarbeiten muss, um die Gefahren, die das kosmetische Mittel für die menschliche Gesundheit darstellen kann, zu identifizieren und zu quantifizieren. In Anhang I finden wir im Detail, welche Elemente die beiden Teile enthalten müssen, nämlich:
TEIL A enthält Informationen zur Sicherheit kosmetischer Produkte, wie z.B.:

- Quantitative und qualitative Zusammensetzung des kosmetischen Mittels;
- Physikalische/chemische Eigenschaften und Stabilität des kosmetischen Mittels;
- Mikrobiologische Qualität;
- Verunreinigungen, Spuren, Informationen über das Verpackungsmaterial;
- Normale und vernünftigerweise vorhersehbare Nutzung;
- Exposition gegenüber dem kosmetischen Mittel;
- Exposition gegenüber den Substanzen;
- Toxikologisches Profil der Substanzen;
- Unerwünschte Wirkungen und schwerwiegende unerwünschte Wirkungen;
- Informationen über das kosmetische Mittel.
Während TEIL B die Sicherheitsbewertung für kosmetische Mittel enthält, nämlich:
- Schlussfolgerung der Bewertung: Erklärung zur Sicherheit des kosmetischen Mittels in Bezug auf Artikel 3;
- Gekennzeichnete Warnhinweise und Gebrauchsanweisungen: Erklärung über die Notwendigkeit, besondere Warnhinweise und Gebrauchsanweisungen gemäß Artikel 19 Absatz 1 Buchstabe d zu kennzeichnen;
- Begründungen: Erläuterung der wissenschaftlichen Argumentation, die zu der in Abschnitt 1 dargelegten Bewertungsschlussfolgerung und der in Abschnitt 2 dargelegten Aussage führt. Diese Erklärung stützt sich auf die Beschreibungen in Teil A. Gegebenenfalls sind die Sicherheitsmargen zu bewerten und zu erörtern. Es gibt unter anderem eine spezifische Bewertung für kosmetische Mittel, die für Kinder unter drei Jahren bestimmt sind, und für kosmetische Mittel, die ausschließlich für die äußere Intimpflege bestimmt sind. Mögliche Wechselwirkungen der in dem kosmetischen Mittel enthaltenen Stoffe müssen bewertet werden. Die Berücksichtigung bzw. Nichtberücksichtigung der verschiedenen toxikologischen Profile ist hinreichend zu begründen. Die Auswirkungen der Stabilität auf die Sicherheit des kosmetischen Mittels sind gebührend zu berücksichtigen.
- Berechtigungsnachweis des Gutachters und Genehmigung von Teil B.

Häufige Irrtümer, die über CPSR gemacht werden
Wir möchten auch einige Beispiele dafür anführen, was häufige Fehler sein können und was uns begegnen kann, wenn wir über CPSR sprechen:
- Der CPSR basiert nur auf der Zusammensetzung der Formel in Inhaltsstoffen (und wird nicht aus der Aufschlüsselung der Rohstoffe neu erstellt);
- Verunreinigungen werden nicht richtig identifiziert;
- Die Art und Bewertung des Verpackungsmaterials ist sehr begrenzt oder sogar nicht vorhanden;
- Wichtige Rohstoffdokumente fehlen (z.B. das IFRA-Zertifikat eines Duftstoffs);
- Die Qualität der Tests ist sehr unzureichend oder negative Testergebnisse werden ignoriert oder unterschätzt;
- Toxikologische Daten zu den einzelnen Inhaltsstoffen liegen nicht oder nur sehr begrenzt vor;
- Die Exposition gegenüber dem Kosmetikprodukt ist zu optimistisch oder sogar völlig falsch;
- Nur die systemische Toxizität wird quantitativ bewertet (nicht immer gut) und andere toxikologische Endpunkte wie Hautsensibilisierung, Hautreizung usw. werden nicht berücksichtigt;
- Der Sicherheitsbewerter verfügt nicht über die richtigen Qualifikationen;
- Der CPSR wird nicht beibehalten, sondern er sollte sich mit dem Produkt weiterentwickeln.
Deshalb ist es wichtig, sich auf einen ehrlichen und zuverlässigen Berater wie Biorius zu verlassen: Unsere Sicherheitsbewerter sind hoch qualifiziert und haben die erforderlichen Abschlüsse erworben, um diese Aufgabe zu erfüllen und den Teil B des CPSR unterzeichnen zu können.
Für weitere Informationen über das CPSR und die von Biorius angebotenen Dienstleistungen zögern Sie bitte nicht, uns zu kontaktieren.

