Introducción

En la parte anterior, se ha destacado que los péptidos y las proteínas son ingredientes cosméticos interesantes, sobre todo por sus actividades antienvejecimiento. Ya existe en el mercado una plétora de materias primas cosméticas a base de péptidos, y se investigan más constantemente.
Hasta ahora, la regulación de estos ingredientes se refiere en gran medida a su origen (deben sintetizarse o extraerse, pero no de células humanas ni de otros organismos) y a las declaraciones de comercialización. La mayoría de las veces, estas afirmaciones no son frívolas, sino que se equilibran con una actividad fisiológica pronunciada, a menudo acompañada de efectos secundarios que deben investigarse. En esta parte, se tratarán los aspectos de seguridad de los péptidos y las proteínas, junto con varias normas generalizadas para garantizar un riesgo limitado para la salud humana al desarrollar o utilizar nuevos péptidos y proteínas en materias primas y productos cosméticos.
Ingredientes de nueva generación frente a los de la generación anterior
Dada su potencial bioactividad, los péptidos y las proteínas han sido objeto de una intensa investigación médica a lo largo de los años. Por tanto, se pueden extraer aspectos relativos a sus propiedades y seguridad y compararlos con moléculas pequeñas definidas químicamente. Esto también es análogo a los cosméticos, ya que muchos ingredientes utilizados durante décadas son pequeñas moléculas definidas químicamente (niacinamida, retinol, etc.), frente a la nueva generación de péptidos y proteínas (factores de crecimiento, subunidades de colágeno, etc.).
Tabla 1: Comparación del perfil entre moléculas pequeñas y péptidos y proteínas
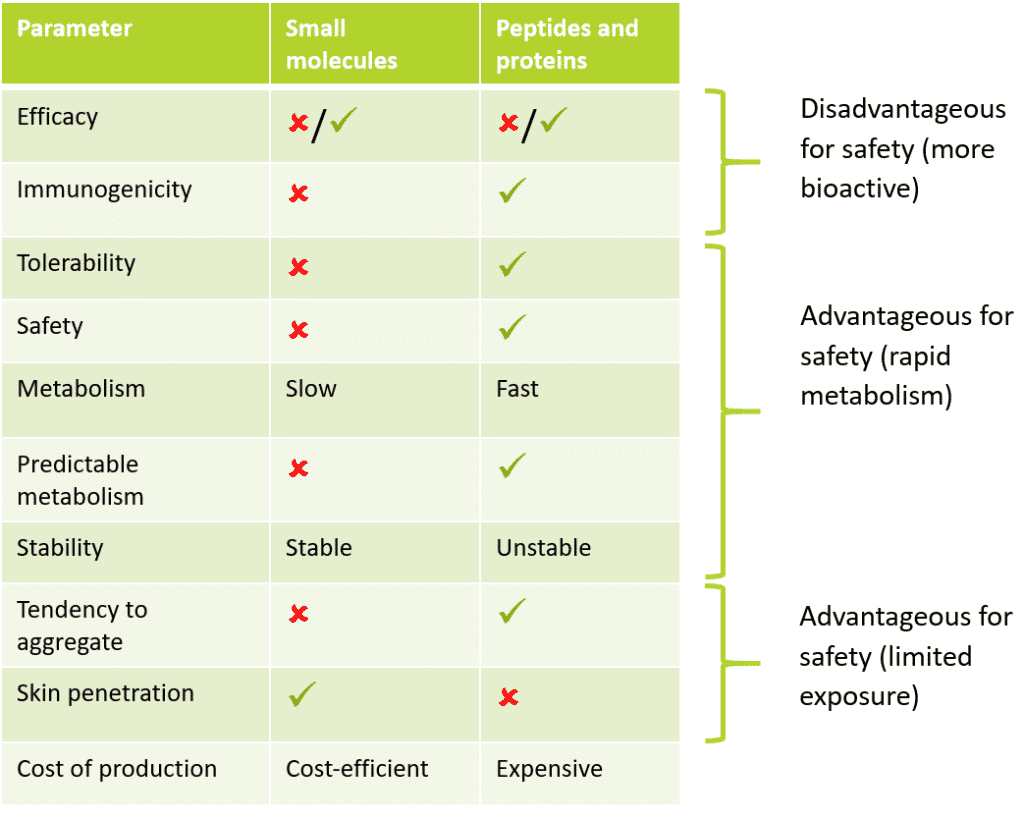
Como se ha visto anteriormente, los péptidos y las proteínas tienen una serie de propiedades intrínsecas que son beneficiosas para un perfil de seguridad mejorado en comparación con las moléculas pequeñas. Por ejemplo, según la investigación farmacéutica, se ha descubierto que los fármacos peptídicos y proteicos tienen un perfil de seguridad mejor y se toleran mejor que sus predecesores tradicionales de moléculas pequeñas. Esto se debió al rápido metabolismo y a la disminución de la estabilidad, lo que redujo la biodisponibilidad y, al mismo tiempo, mantuvo menos efectos fuera del objetivo.
En el ámbito de los cosméticos, esta menor biodisponibilidad conlleva un menor riesgo para la seguridad. El fundamento de esto es el dogma central de la toxicología: “la dosis hace el veneno” – Paracelso 1500, considerado como el padrino de la toxicología. Las propiedades que se prestan a una menor toxicidad asociada a los péptidos y las proteínas en comparación con las moléculas pequeñas se tratarán a continuación por punto final toxicológico, muchos de estos puntos finales constituyen la base de la evaluación toxicológica de cualquier ingrediente.
Absorción, distribución, metabolismo y excreción

La absorción, distribución, metabolismo y excreción (o ADME) son los principales procesos que definen la exposición a sustancias exógenas. En cuanto a los cosméticos, esto se debe principalmente a la absorción dérmica, dado que los cosméticos se aplican normalmente por vía dérmica y la piel es en realidad una barrera importante para las sustancias exógenas.
La piel está formada por varias capas, la más superficial de las cuales es el estrato córneo, formado por células queratinizadas apretadas que sirven de barrera importante a la entrada de sustancias grandes y/o hidrófilas.
Los péptidos suelen tener pesos moleculares de altos a muy altos y suelen estar cargados a pH fisiológico, lo que los hace hidrófilos, contribuyendo así a su escasa permeación cutánea pasiva. Además, los péptidos contienen múltiples enlaces amida (como grupos donantes y aceptores de enlaces de hidrógeno) que pueden afectar a su difusión a través de la piel.
Otro aspecto que merece consideración es que el metabolismo y la actividad proteolítica de la piel son potencialmente importantes para la administración transcutánea de péptidos. La piel contiene sistemas enzimáticos comparables a los de otros tejidos, por ejemplo el hígado. Las enzimas endógenas como las deaminasas, las esterasas y las aminopeptidasas se encuentran en todos los compartimentos de la piel y pueden contribuir al metabolismo rápido de los péptidos y las proteínas antes de entrar en la circulación sistémica, suponiendo que estos péptidos y proteínas hayan podido incluso atravesar el estrato córneo inicialmente.
Como tal, la piel sirve de barrera importante para los péptidos y las proteínas en función del tamaño de estas moléculas y de la capacidad metabólica de la piel, lo que conduce a una exposición sistémica limitada. Un ejemplo que lo demuestra mejor es quizás el del pentapéptido-4 (KTTKS) que, a pesar de ser un péptido de sólo 5 aminoácidos, se descubrió que no estaba presente en el fluido receptor ni en ninguna de las capas de la piel (el estrato córneo, la epidermis y la dermis) en la piel de ratones sin pelo (Choi et al., 2014).
Fototoxicidad

El potencial de fototoxicidad puede identificarse basándose en parámetros in silico. Por un lado, el coeficiente de extinción -la capacidad de una sustancia para absorber la luz- puede utilizarse como indicador del riesgo potencial. Por ejemplo, las sustancias con coeficientes de extinción inferiores a 1 000 L mol-1 cm-1 se consideran de menor riesgo fototóxico, ya que es poco probable que este bajo nivel de absorción de la luz resulte perjudicial (Henry et al., 2009). Esta opinión también la comparten la IHC (Conferencia Internacional de Armonización, 2013) y la Agencia Europea del Medicamento (Agencia Europea de Medicamentos, 2011).
Específicamente para los péptidos y las proteínas, existen varias herramientas basadas en Internet capaces de predecir los coeficientes de extinción basándose en la presencia de residuos de tirosina, triptófano y cisteína, aminoácidos conocidos por absorber la luz. Por ello, limitar los residuos de tirosina, triptófano y cisteína puede limitar radicalmente el coeficiente de extinción de la proteína o el péptido y, por tanto, limitar el riesgo de fototoxicidad.
Genotoxicidad

En general, no se espera que los péptidos y las proteínas sean potencialmente genotóxicos. En una de sus directrices (ICH S6(R1)), el ICH (Consejo Internacional de Armonización de los Requisitos Técnicos para los Productos Farmacéuticos de Uso Humano) afirma que “no se espera que estas sustancias (péptidos/proteínas) interactúen directamente con el ADN u otro material cromosómico” (Conferencia Internacional de Armonización, 2011). Esto se confirmó en otros estudios en los que se probó la genotoxicidad de 78 proteínas y sólo cuatro parecían provocar efectos genotóxicos reproducibles.
La actividad de uno de estos péptidos se atribuyó a su molécula enlazadora, mientras que no se pudo establecer un fundamento claro para los 3 péptidos restantes, salvo una posible actividad enzimática/hormonal. De hecho, se llegó a la conclusión de que, para la proteína “media”, las reacciones electrofílicas son difíciles de prever (Gocke et al., 1999).
No obstante, esto demuestra que debe prestarse mucha atención a los procesos de producción utilizados para producir estos péptidos y proteínas, ya que algunos reactivos pueden ser genotóxicos, mientras que es necesario incorporar pasos de purificación en los procesos de producción para limitar el arrastre de posibles subproductos a la materia prima.
Sensibilización

El tipo de sensibilización más importante para los productos cosméticos es la dermatitis de contacto, que se clasifica como sensibilización de tipo 4 e implica sobre todo a las células T. En general, se acepta que los sensibilizadores cutáneos son electrófilos y capaces de reaccionar con los grupos nucleófilos de las proteínas, como las unidades de cisteína y lisina.
Otro mecanismo importante se basa en las reacciones de los radicales libres (Roberts et al., 2012). Dado que ambos tipos de reacciones son improbables con el péptido investigado y que se espera que la absorción de dicho compuesto sea baja, el riesgo de sensibilización cutánea se considera bajo.
Sin embargo, dado que muchas proteínas y péptidos presentes en los alimentos también sirven como alérgenos, las proteínas y los péptidos utilizados en los cosméticos merecían ser evaluados para detectar este tipo de alergenicidad. Concretamente, en la hipersensibilidad inmediata, como la alergia y la anafilaxia, intervienen mecanismos diferentes en comparación con la dermatitis de contacto.
En la sensibilización de tipo 1, las células efectoras son principalmente células productoras de anticuerpos, como los mastocitos y los anticuerpos IgE. Sin embargo, de los dictámenes científicos del CCSC y del CIR sobre las proteínas de trigo hidrolizadas, se desprende que los péptidos con un peso molecular inferior a 3,5 kDa tienen una baja capacidad de sensibilización (CCSC, 2014). Por ello, para que se produzca una reacción de sensibilización de tipo 1, un alérgeno debe unirse a dos anticuerpos IgE. Por tanto, un alérgeno debe contener al menos dos sitios de unión de IgE, cada uno con una longitud mínima de 15 aminoácidos. Esto implica que el tamaño mínimo de los alérgenos proteicos es de aproximadamente 30 aminoácidos (Huby, 2000).
Peligro potencial para la salud humana

Basándonos en lo expuesto anteriormente, se podría suponer que los péptidos y las proteínas no tienen perfiles toxicológicos significativos, lo cual sería incorrecto. De hecho, los péptidos y las proteínas pueden albergar un peligro para la salud humana que se debe a la biodisponibilidad y a una farmacología exagerada. Por ejemplo, las proteínas en forma de receptores y enzimas se consideran la unidad funcional que facilita las funciones corporales normales. Lo mismo ocurre con los péptidos que incluyen moléculas de señalización. Por ello, si se produjera un desequilibrio en la homeostasis por aumento o disminución de la actividad, podrían surgir efectos adversos. Sin embargo, la identificación de estos acontecimientos “farmacológicos exagerados” no es fácil en los enfoques actuales de las pruebas de seguridad.
Para identificar el peligro potencial para la salud humana, y dada la naturaleza de las proteínas y los péptidos en el sentido de que, podría producirse una cascada de acontecimientos biológicos que podrían dar lugar a un efecto adverso, sería necesario un enfoque holístico. Para ello, podría preverse que las tecnologías ómicas de nueva generación serían de gran ayuda. En resumen, estas tecnologías permiten una visión global de los acontecimientos moleculares que se producen a nivel de genes y proteínas. Una vez identificada una red de genes y/o proteínas afectados, ésta puede vincularse a modos de acción moleculares que se sabe que dan lugar a efectos adversos para la salud. Esto está en consonancia con el enfoque de la Vía de Resultados Adversos (VEA), en el que se predicen los efectos adversos apicales para la salud a partir de los acontecimientos moleculares iniciadores, un enfoque que está ganando mucho terreno en la toxicología reguladora. Para ponerlo en práctica con éxito sería necesario desarrollar competencias en estos campos, al tiempo que se garantiza que las pruebas no resulten prohibitivas desde el punto de vista de los costes. Además, algunos POA se han desarrollado y validado, mientras que otros se encuentran en distintas fases de aceptación y desarrollo. De hecho, aún queda mucho trabajo por hacer para mapear las vías moleculares toxicológicas como AOPs. Por ello, dado que todavía no se puede identificar fácilmente el peligro para la salud humana utilizando estos enfoques, la incertidumbre se gestiona garantizando la biodisponibilidad limitada de estos ingredientes cosméticos.
Conclusión

Como se ha descrito anteriormente, los péptidos y las proteínas se benefician de una serie de propiedades que podrían limitar el riesgo para la salud. Estas propiedades son especialmente importantes a la luz de la prohibición de las pruebas con animales para los ingredientes cosméticos. No obstante, deben evitarse las modificaciones significativas de estos ingredientes para mantener estas características. Estos incluyen brevemente:
- Ninguna modificación extensa para aumentar significativamente la absorción – esto sirve para mantener el dogma central de la toxicología; exposición limitada = riesgo limitado
- Modificaciones limitadas de los aminoácidos – no se espera que los aminoácidos naturales sean genotóxicos, carcinógenos ni tóxicos para la reproducción mientras se metabolizan rápidamente
- Limitar la cantidad de residuos de tirosina, triptófano y cisteína – Limitar el potencial de fototoxicidad
- Incluir fases de purificación en los procesos de producción – para limitar el arrastre de impurezas potencialmente peligrosas
Estas consideraciones son importantes a la luz de la prohibición de los ensayos con animales para los ingredientes cosméticos, en los que los toxicólogos tienen que basarse en datos y herramientas distintos de los ensayos toxicológicos tradicionales con animales. Además, como se menciona en la Parte I, los cosméticos y los medicamentos se distinguen en función de sus usos previstos, que se rigen principalmente por sus alegaciones. Sin embargo, según el manual del Grupo de Trabajo de Productos Cosméticos sobre productos límite, las sustancias que restauran, corrigen o modifican las funciones fisiológicas ejerciendo actividades farmacológicas se identifican “en virtud de su presentación” (según las reivindicaciones descritas anteriormente) o “en virtud de su función”. Esta última “se evalúa teniendo en cuenta todas las características del producto, como la absorción, la concentración, la vía de administración, la frecuencia de aplicación, el lugar de aplicación y el grado de penetración”. Por ello, resulta obvio el papel que desempeña comprender cómo se entrelazan las características de los péptidos y las proteínas para impulsar los perfiles toxicológicos a la hora de determinar cuándo un ingrediente es un fármaco o un cosmético.
Referencias
Choi, Y.L., Park, E.J., Kim, E., Na, D.H. y Shin, Y.H. (2014). Estabilidad dérmica y permeación cutánea in vitro de pentapéptidos de colágeno (KTTKS y palmitoil-KTTKS). Biomol. Ter. 22, 321-327.
Agencia Europea de Medicamentos (2011). Preguntas y respuestas sobre la ‘ Nota orientativa de los ensayos de fotoseguridad’.
Gocke, E., Albertini, S., Brendler-Schwaab, S., Müller, L., Suter, W., y Würgler, F.E. (1999). Pruebas de genotoxicidad de los productos derivados de la biotecnología: Informe de un grupo de trabajo de la GUM. Mutat. Res. – Rev. Mutat. Res. 436, 137-156.
Henry, B., Foti, C., y Alsante, K. (2009). ¿Pueden utilizarse los datos de absorción de luz y fotoestabilidad para evaluar los riesgos de fotoseguridad en pacientes de una nueva molécula de fármaco? J. Photochem. Fotobiol. B Biol. 96, 57-62.
Huby, R.D.J. (2000). ¿Por qué algunas proteínas son alergénicas? Toxicol. Sci. 55, 235-246.
Conferencia Internacional sobre Armonización (2011). Evaluación preclínica de la seguridad de los productos farmacéuticos derivados de la biotecnología.
Conferencia Internacional sobre Armonización (2013). Evaluación de la fotoseguridad de los productos farmacéuticos.
Roberts, D.W., Basketter, D., Kimber, I., White, J., McFadden, J., y White, I.R. (2012). El metabisulfito sódico como alérgeno de contacto: un ejemplo de mecanismo químico poco frecuente de modificación de proteínas. Dermatitis de Contacto 66, 123-127. SCCS (2014). Opinión sobre las proteínas de trigo hidrolizadas.
Este artículo fue escrito por el Dr. Boris Krivoshiev, antiguo Toxicólogo Principal, durante su etapa en BIORIUS.


