Los Productos Sanitarios constituyen un campo muy complejo en Europa, que genera miles de millones de beneficios. Las variedades y categorías son numerosas, mientras que su uso siempre conlleva grandes riesgos para la seguridad humana. Todos estos factores hacen que el marco de los Productos Sanitarios sea confuso, sobre todo porque está en constante evolución. En la actualidad, la UE está modificando profundamente su normativa sobre Productos Sanitarios y las marcas deben prestar mucha atención al impacto que tendrá en su actividad en los próximos años.
Por otro lado, las herramientas de belleza despiertan cada vez más interés entre los consumidores europeos, deseosos de probar la tecnología más novedosa disponible en el mercado. Las herramientas de belleza podrían clasificarse como Productos Sanitarios, Productos Sanitarios sin una finalidad médica prevista o Productos de Uso General, por lo que su clasificación es un primer paso en su proceso de comercialización y desarrollo. Si tu herramienta de belleza es un Producto Sanitario con o sin finalidad médica, estará regulado por un conjunto de normativas complejas con un largo proceso a seguir antes de poder venderlos. Sumerjámonos en este fascinante tema, ¡que sigue siendo complicado incluso para los profesionales del sector! Con sus expertos dedicados a los Productos Sanitarios, BIORIUS está siempre al tanto de las últimas novedades en Europa.
Instrumentos de belleza: ¿cómo saber si son productos sanitarios en la UE?
Aunque categorizar las herramientas de belleza parece una tarea fácil al principio, muchas marcas están luchando con esta cuestión clave.
Según las normas de la UE, una El Producto Sanitario debe responder a un problema médico o a una enfermedad, que se curaría, trataría o diagnosticaría gracias a la acción del producto. El modo de funcionamiento debe ser físico porque no debes confundir un Producto Sanitario con un medicamento. Aunque su acción auxiliar puede ser medicinal o metabólica (por ejemplo, distribuir un medicamento en el organismo), su finalidad principal no puede serlo.
En consecuencia, la primera pregunta que debes hacerte para clasificar tu herramienta de belleza es ¿Mi producto muestra una alegación médica y aborda físicamente el problema?
- Ejemplo de herramienta de belleza clasificada como Producto Sanitario: Máscara de luz LED que previene el acné grave o la rosácea.
- Ejemplo de herramienta de belleza clasificada como Producto de uso general: Rodillo facial de microcorriente
ATENCIÓN: la definición de Producto Sanitario no es la misma en todo el mundo. China, EE.UU. y otros países tienen normas diferentes; los rodillos faciales de microcorriente están clasificados como Productos Sanitarios en EE.UU., por ejemplo (código de producto OUH).
Reglamentos de la UE sobre productos sanitarios y productos sanitarios sin una finalidad médica prevista
La nueva normativa de la UE sobre productos sanitarios
En la Unión Europea, los Productos Sanitarios se dividen en dos categorías diferentes: Productos Sanitarios “normales” (MDR) y Productos Sanitarios para Diagnóstico In Vitro (IVDR). Su marco jurídico se modificó drásticamente en 2017, cuando se adoptaron dos nuevos reglamentos: el Reglamento (UE) 2017/745 para los MDR y el Reglamento (UE) 2017/746 para los IVDR. El objetivo era adaptarse a los cambios tecnológicos contemporáneos, reforzar las normas, evitar cualquier interpretación y armonizar las prácticas entre la UE y los países internacionales.
¿Y en el Reino Unido? Son aplicables en el Reino Unido como medida temporal. Las autoridades británicas están decidiendo actualmente una normativa específica que sustituya a las de la UE, mientras que a partir de julio de 2023 empezará a exigirse un marcado diferente (UKCA).
Los instrumentos de belleza y los cosméticos clasificados como Productos Sanitarios se consideran MDR, pero se hacen otras distinciones entre ellos. De hecho, las MDR se clasifican en Clase I, Clase IIa, Clase IIb y Clase III, de bajo a alto riesgo. Cada clasificación conlleva requisitos específicos, como las obligaciones del fabricante, la obligación de un Organismo Notificado o un registro adicional en algunos Estados miembros de la UE.
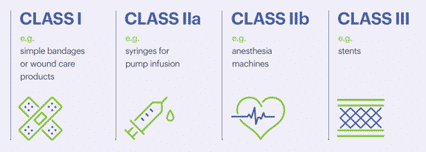
Tus utensilios de belleza o cosméticos pueden clasificarse de la Clase I a la Clase III, la más regulada y la que requiere más tiempo. Si quieres ayuda para definir la clasificación de tu producto, BIORIUS está aquí para ayudarte.
Por tanto, las marcas deben tener en cuenta los requisitos específicos de la Clase, así como la nueva normativa que ha entrado en vigor recientemente con un periodo de adaptación hasta 2025. Sin embargo, el infame anexo XVI del Reglamento (UE) 2017/745 aún no se aplica, pero cambiará drásticamente la faz del mercado europeo para los fabricantes afectados…
Productos sanitarios sin finalidad médica prevista
Además de la definición anterior, un Producto Sanitario puede no tener una finalidad médica prevista. Esta categoría límite incluye los cosméticos y los instrumentos de belleza que presentan inicialmente una acción estética o una finalidad médica “oculta” como estética. Por razones de seguridad, se añadieron 6 grupos de productos en el anexo XVI del Reglamento (UE) 2017/745, para ser considerados Productos Sanitarios sin una finalidad médica prevista. Cada clasificación estará sujeta a requisitos específicos. Este anexo XVI aún no ha salido oficialmente porque todavía faltan los requisitos específicos (Especificaciones Comunes), pero se cree que saldrá antes de finales de 2022.
Ya escribimos un artículo sobre este tema, pero a modo de recordatorio aquí tienes los 6 productos a los que va dirigido este Anexo:
- Lentes de contacto u otros objetos que se introduzcan en el ojo o sobre él.
- Productos destinados a ser introducidos total o parcialmente en el cuerpo humano por medios quirúrgicamente invasivos con el fin de modificar la anatomía o fijar partes del cuerpo, con excepción de los productos para tatuajes y los piercings –> Implantes…
- Sustancias, combinaciones de sustancias o artículos destinados a ser utilizados para el relleno facial o de otras membranas dérmicas o mucosas mediante inyección subcutánea, submucosa o intradérmica u otra introducción, excluidos los de tatuaje –> Rellenos dérmicos, microagujas y herramientas de mesoterapia.
- Aparatos destinados a reducir, eliminar o destruir tejido adiposo, como los aparatos de liposucción, lipólisis o lipoplastia.
- Aparatos emisores de radiaciones electromagnéticas de alta intensidad destinados a ser utilizados sobre el cuerpo humano, incluidas las fuentes coherentes y no coherentes, monocromáticas y de amplio espectro, como los láseres y los aparatos de luz pulsada intensa, para el rejuvenecimiento de la piel, la eliminación de tatuajes o del vello u otros tratamientos cutáneos–> Aparatos de depilación por LED.
- Equipos destinados a la estimulación cerebral que aplican corrientes eléctricas o campos magnéticos o electromagnéticos que penetran en el cráneo para modificar la actividad neuronal del cerebro –> Tratamiento de la depresión…

ATENCIÓN: podrían añadirse al Anexo XVI categorías adicionales de productos que puedan inducir un riesgo. Si tu herramienta cosmética o de belleza está en el Anexo XVI, o si crees que podría incluirse en él en el futuro, debes prepararte para cumplir la normativa ahora.
Si vendo cosméticos o herramientas de belleza considerados Productos Sanitarios, ¿tengo tiempo para cumplir la nueva normativa de la UE y el Anexo XVI?
La respuesta es sí, gracias a los periodos transitorios. Se implementaron para concederte tiempo suficiente durante el cual deberías decidir proceder y empezar a realizar los estudios requeridos y a introducir cualquier cambio necesario. No obstante, debes tener en cuenta que
- Todas las marcas y fabricantes tienen de plazo hasta 2024 antes de que pierda su validez el certificado concedido con arreglo a la antigua normativa sobre productos sanitarios. Miles de empresas ya están intentando cumplir el Reglamento (UE) 2017/745 y otras miles esperarán al último minuto para hacerlo. Es de esperar que el proceso dure más tiempo, ya 18 meses de media.
- Los fabricantes de cosméticos y utensilios de belleza también deberán cumplir el Anexo XVI una vez que se implante, pero todavía existen incertidumbres. Así, si esperas hasta el último momento, como otras miles de empresas, los largos tiempos de proceso podrían impedirte poner tu producto en el mercado de acuerdo con tu plazo inicial.
Combinados estos dos factores, conseguir la aprobación de tu Organismo Notificado (si necesitas uno) podría llevar hasta varios años. De hecho, además de los Organismos Notificados sobrecargados de trabajo y las prisas esperadas, los Productos Sanitarios sin una finalidad médica prevista no son la prioridad. Los Productos Sanitarios habituales esenciales para la seguridad humana o la asistencia sanitaria se tratarán en primer lugar y el resto pueden ser los últimos de la fila.

¡No esperes más! BIORIUS puede ayudarte a desarrollar tu DM proporcionándote servicios de Responsable UE/Reino Unido (para empresas con sede fuera de Europa), vigilancia poscomercialización, clasificación MDR o creación de tu documentación técnica. También podemos ayudarte a elegir tu Organismo Notificado, si lo necesitas. Para cumplir los últimos cambios normativos, podemos confirmar tu clasificación de DM, actualizar tu evaluación de bioseguridad o analizar el desfase entre tu sistema actual y la nueva normativa. Si quieres vender un Producto Sanitario sin finalidad médica, también podemos proporcionarte asistencia de la A a la Z.
¡Trabajar con nosotros te hará ahorrar tiempo y dinero! ¿Tienes alguna petición especial? No dudes en ponerte en contacto con nosotros para poner en marcha soluciones a medida: info@biorius.com


