はじめに

前編では、ペプチドとタンパク質が、特にアンチエイジング活性の点で、興味深い化粧品成分であることが強調された。 ペプチドベースの化粧品原料はすでに市場に多数出回っており、さらに多くの原料が絶えず研究されている。
これまでのところ、これらの成分に関する規制の大部分は、その起源(合成または抽出されたものでなければならないが、ヒト細胞やその他の生物から抽出されたものであってはならない)と販売表示に関するものである。 たいていの場合、こうした主張は軽薄なものではなく、顕著な生理学的活性と釣り合いが取れており、しばしば調査しなければならない副作用を伴う。 このパートでは、ペプチドとタンパク質の安全性の側面について、化粧品原料や製品に新しいペプチドとタンパク質を開発または使用する際に、ヒトの健康に対するリスクが限定的であることを保証するためのいくつかの一般的なルールとともに議論する。
次世代成分と旧世代成分の比較
ペプチドとタンパク質は、その潜在的な生理活性から、長年にわたって激しい医学研究の対象となってきた。 そのため、その特性や安全性に関する側面を引き出し、化学的に定義された低分子と比較することができる。 数十年にわたって使われてきた成分の多くが化学的に定義された低分子(ナイアシンアミド、レチノールなど)であるのに対し、次世代のペプチドやタンパク質(成長因子、コラーゲンサブユニットなど)は化学的に定義された低分子であるからだ。
表1:低分子化合物とペプチドおよびタンパク質のプロファイルの比較
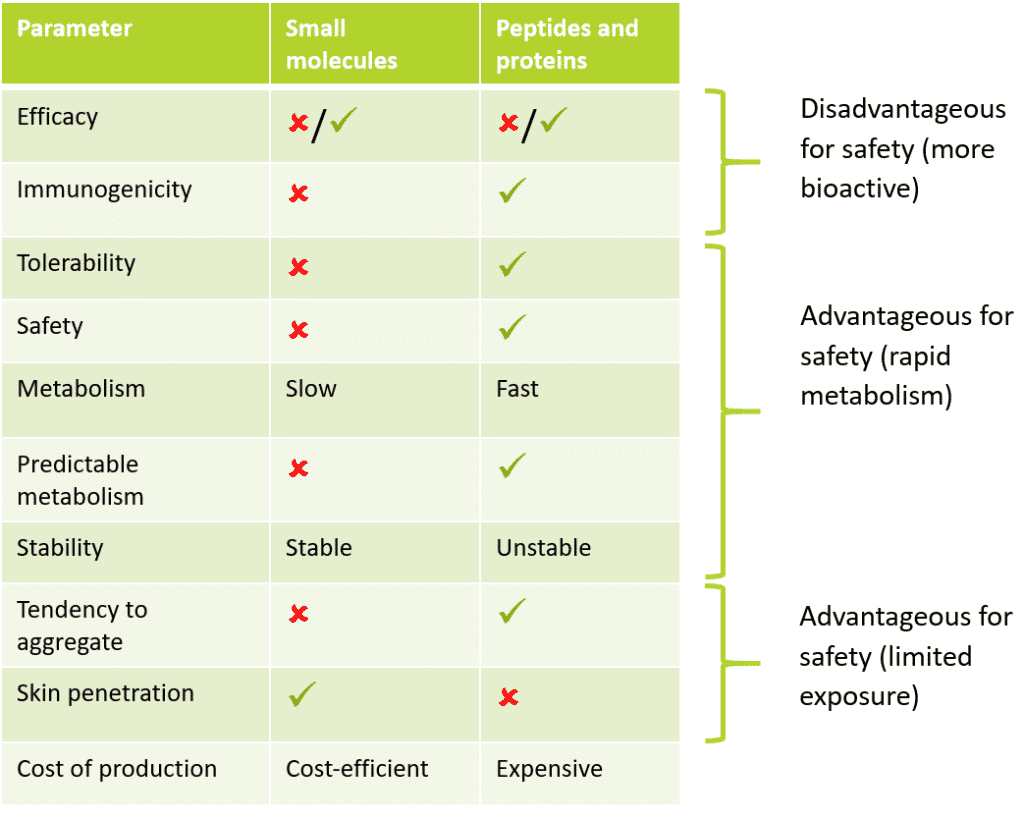
以上のように、ペプチドやタンパク質には、低分子化合物と比較して安全性プロファイルを向上させるために有益な、多くの固有の特性がある。 例えば、製薬会社の研究によれば、ペプチドやタンパク質の医薬品は、従来の低分子医薬品よりも安全性が高く、忍容性が高いことが判明している。 これは、代謝が早く、安定性が低下しているためで、バイオアベイラビリティが低下する一方、標的外作用は少なく保たれている。
化粧品の範囲では、このバイオアベイラビリティの低下は、安全性に対するリスクの低下につながる。 その根拠となるのが、毒物学のセントラルドグマである:「毒物学の名付け親とされる1500年代のパラケルスス。 低分子化合物と比較して、ペプチドやタンパク質の毒性が低いという特性については、毒性学的エンドポイントごとに後述するが、これらのエンドポイントの多くは、あらゆる成分の毒性学的評価の基礎となるものである。
吸収、分布、代謝、排泄

吸収、分布、代謝、排泄(またはADME)は、外因性物質への曝露を規定する主なプロセスである。 化粧品に関しては、化粧品は通常経皮的に塗布され、皮膚は外因性物質に対する重要なバリアであることから、これは主に経皮吸収によるものである。
皮膚はさまざまな層で構成されているが、その最表層に位置するのが角質層で、密に詰まったケラチン化細胞からなり、大きな物質や親水性物質の侵入を防ぐ重要なバリアとなっている。
ペプチドは一般的に高分子量から超高分子量であり、生理的pHでは一般的に親水性に帯電するため、皮膚透過性が悪くなる。 加えて、ペプチドには複数のアミド結合(水素結合のドナー基とアクセプター基として)があり、これが皮膚上での拡散に影響を与える可能性がある。
もうひとつ考慮すべき点は、皮膚の代謝とタンパク質分解活性が、ペプチドの経皮デリバリーにとって重要な意味を持つ可能性があるということだ。 皮膚には、肝臓など他の組織に見られるものと同等の酵素系が存在する。 デアミナーゼ、エステラーゼ、アミノペプチダーゼなどの内因性酵素は、皮膚のあらゆる部位に存在し、これらのペプチドやタンパク質が最初に角質層を通過できたと仮定すると、全身循環に入る前に、ペプチドやタンパク質の迅速な代謝に寄与している可能性がある。
このように、皮膚は、ペプチドやタンパク質の分子サイズと皮膚の代謝能力から、重要なバリアとして機能し、全身への暴露を制限している。 このことを最もよく示す例は、ペンタペプチド-4(KTTKS)であろう。このペンタペプチド-4は、わずか5アミノ酸のペプチドであるにもかかわらず、ヘアレスマウスの皮膚では、受容体液にも皮膚層(角質層、表皮、真皮)にも存在しないことが判明した(Choi et al, 2014)。
光毒性

光毒性の可能性は、in silicoパラメータに基づいて特定することができる。 ひとつは、消衰係数(物質が光を吸収する能力)が潜在的リスクの指標として使えることだ。 例えば、消衰係数が1,000 L mol-1 cm-1未満の物質は、この低レベルの光吸収率では有害となる可能性が低いため、光毒性のリスクは低いと判断される(Henry et al.) この意見は、IHC(国際医薬品規制調和会議、2013年)や欧州医薬品庁(欧州医薬品庁、2011年)でも共有されている。
特にペプチドやタンパク質については、光を吸収することが知られているアミノ酸であるチロシン、トリプトファン、システイン残基の存在に基づいて消光係数を予測できるウェブベースのツールが数多くある。 そのため、チロシン、トリプトファン、システイン残基を制限することで、タンパク質やペプチドの消衰係数を根本的に制限することができ、光毒性のリスクを抑えることができる。
遺伝毒性

一般的に、ペプチドやタンパク質は遺伝毒性を持つ可能性はないと考えられている。 ICH(International Council for Harmonization of Technical Requirements for Pharmaceuticals for Human Use)は、そのガイドラインのひとつ(ICH S6(R1))において、「これらの物質(ペプチド/タンパク質)がDNAやその他の染色体物質と直接相互作用することは想定されていない」と述べている(International Conference on Harmonisation, 2011)。 このことは、他の研究でも確認されている。78種類のタンパク質について遺伝毒性試験を行ったところ、再現性のある遺伝毒性作用を示したのはわずか4種類であった。
これらのペプチドのうち1つの活性はリンカー分子に起因するものであったが、残りの3つのペプチドについては、酵素/ホルモン活性の可能性を除いては、明確な根拠は確立できなかった。 実際、「平均的な」タンパク質では、求電子反応は想定しにくいと結論づけられた(Gockeら、1999年)。
とはいえ、試薬の中には遺伝毒性を持つものもあるため、これらのペプチドやタンパク質を製造する際には、製造工程に大きな注意を払う必要がある。また、潜在的な副産物の原料へのキャリーオーバーを抑えるためには、製造工程に精製ステップを組み込む必要がある。
感作

化粧品に対する感作の最も重要なタイプは接触皮膚炎で、これはタイプ4の感作に分類され、ほとんどがT細胞に関与する。 一般に、皮膚感作剤は親電性であり、システインやリジンなどのタンパク質上の求核基と反応する。
もうひとつの重要なメカニズムは、フリーラジカル反応に基づくものである(Roberts et al.) 調査対象のペプチドでは、どちらの反応も起こりにくく、このような化合物の吸収は低いと予想されるため、皮膚感作性のリスクは低いと考えられる。
しかし、食品に含まれる多くのタンパク質やペプチドがアレルゲンとなることを考えると、化粧品に使用されるタンパク質やペプチドは、この種のアレルゲン性を評価する必要がある。 特に、アレルギーやアナフィラキシーのような即時型過敏症は、接触皮膚炎とは異なるメカニズムを伴う。
1型感作では、エフェクター細胞のほとんどが肥満細胞やIgE抗体などの抗体産生細胞である。 しかし、加水分解小麦タンパク質に関するSCCSとCIRの科学的見解から、分子量3.5kDa以下のペプチドは感作性が低いことが明らかになっている(SCCS, 2014)。 このように、1型感作反応が起こるためには、アレルゲンは2つのIgE抗体と結合しなければならない。 したがって、アレルゲンは少なくとも2つのIgE結合部位を持ち、それぞれが最低15アミノ酸長でなければならない。 このことは、タンパク質アレルゲンの最小サイズは約30アミノ酸であることを示唆している(Huby, 2000)。
人の健康に対する潜在的危険性

上述したことから、ペプチドやタンパク質には重要な毒性プロファイルはないと思われるかもしれないが、それは間違いである。 実際、ペプチドやタンパク質は、バイオアベイラビリティや誇張された薬理作用によって、人の健康に害を及ぼす可能性がある。 例えば、受容体や酵素の形をしたタンパク質は、正常な身体機能を促進する機能単位と考えられている。 シグナル分子を含むペプチドも同様だ。 そのため、活動の増減によってホメオスタシスのバランスが崩れれば、悪影響が生じる可能性がある。 しかし、このような「薬理学的に誇張された」事象を特定することは、現在の安全性試験のアプローチでは容易ではない。
ヒトの健康に対する潜在的な危険性を特定するためには、また、タンパク質やペプチドの性質として、有害な影響につながりうる生物学的事象のカスケードが起こりうることを考えると、総合的なアプローチが必要となる。 そのためには、次世代のオミックス技術が大いに役立つことが想定される。 簡単に言えば、これらの技術によって、遺伝子やタンパク質レベルで起こる分子事象を包括的に概観することができる。 影響を受ける遺伝子やタンパク質のネットワークが特定されれば、健康への悪影響が生じることが分かっている分子作用様式と結びつけることができる。 これは、分子レベルの有害事象を起点に健康への悪影響を予測するという、有害事象経路(AOP)アプローチに沿ったものであり、規制毒性学で大きな支持を得ているアプローチである。 これを成功させるには、テストがコスト高にならないようにしつつ、これらの分野のスキルを向上させる必要がある。 さらに、いくつかのAOPは開発され、検証されているが、他のAOPは様々な段階で受け入れられ、開発されている。 実際、毒性学的分子経路をAOPとしてマッピングするには、まだかなりの量の作業が必要である。 そのため、これらのアプローチではヒトの健康への有害性を容易に特定することができないことから、これらの化粧品成分の限定的な生物学的利用能を確保することで不確実性を管理している。
結論

上述したように、ペプチドとタンパク質は、健康リスクを制限しうる多くの特性を持っている。 これらの特性は、化粧品成分の動物実験禁止の観点から特に重要である。 とはいえ、これらの特徴を維持するためには、これらの成分に大幅な変更を加えることは避けるべきである。 簡単に説明すると、以下のようなものだ:
- 吸収率を著しく高めるような大がかりな改良はしない-これは毒物学のセントラルドグマを維持するためである。
- アミノ酸への修飾を制限 – 天然アミノ酸は、急速に代謝される一方で、遺伝毒性、発がん性、生殖毒性はないと予想される。
- チロシン、トリプトファン、システイン残基の量を制限する – 光毒性の可能性を制限する
- 潜在的に危険な不純物のキャリーオーバーを抑制するため、製造工程に精製工程を含める。
化粧品成分の動物実験が禁止され、毒物学者が従来の動物毒性試験以外のデータやツールに頼らざるを得なくなったことを考えると、こうした配慮は重要である。 さらに、第一部で述べたように、化粧品と医薬品は、主にその謳い文句に左右される使用目的に基づいて区別される。 ただし、化粧品ワーキンググループのボーダーライン製品に関するマニュアルに基づき、薬理活性を発揮して生理機能を回復、修正、変更する物質は、「表示によるもの」(上記のようなクレーム)、または「機能によるもの」で識別される。 後者は、「吸収、濃度、投与経路、適用頻度、適用部位、浸透の程度など、製品のあらゆる特性を考慮して評価」される。 このように、ある成分が医薬品か化粧品かを判断する際に、ペプチドとタンパク質の特性がどのように絡み合って毒性学的プロファイルをもたらすかを理解する役割は明白である。
参考文献
Choi, Y.L., Park, E.J., Kim, E., Na, D.H., and Shin, Y.H. (2014). コラーゲンペンタペプチド(KTTKSおよびパルミトイル-KTTKS)の皮膚安定性およびin vitro皮膚透過性。 Biomol. Ther.22, 321-327.
欧州医薬品庁(2011)。 光安全性試験のガイダンス用ノート」に関する質問と回答。
Gocke, E., Albertini, S., Brendler-Schwaab, S., Müller, L., Suter, W., and Würgler, F.E. (1999). バイオテクノロジー由来製品の遺伝毒性試験:GUMタスクフォース報告書。 ミュータット レスがある。 – Rev. Mutat. Res.436, 137-156.
Henry, B., Foti, C., and Alsante, K. (2009). 光吸収と光安定性のデータは、新薬分子の患者における光安全性リスクの評価に使用できるか? J.Photochem. Photobiol. B Biol.96, 57-62.
Huby, R.D.J. (2000). なぜ一部のタンパク質がアレルゲンなのか? Toxicol. 55, 235-246.
ハーモナイゼーション国際会議(2011年)。 バイオテクノロジー由来の医薬品の前臨床安全性評価。
ハーモナイゼーション国際会議(2013年)。 医薬品の光安全性評価。
Roberts, D.W., Basketter, D., Kimber, I., White, J., McFadden, J., and White, I.R. (2012). 接触アレルゲンとしてのメタ重亜硫酸ナトリウム-タンパク質修飾の稀な化学的メカニズムの一例。 接触皮膚炎66, 123-127. SCCS(2014年)。 加水分解小麦タンパク質に関する意見。
この記事は、元主任毒物学者のボリス・クリボシエフ博士がBiorius在籍中に執筆したものである。


