規制の背景
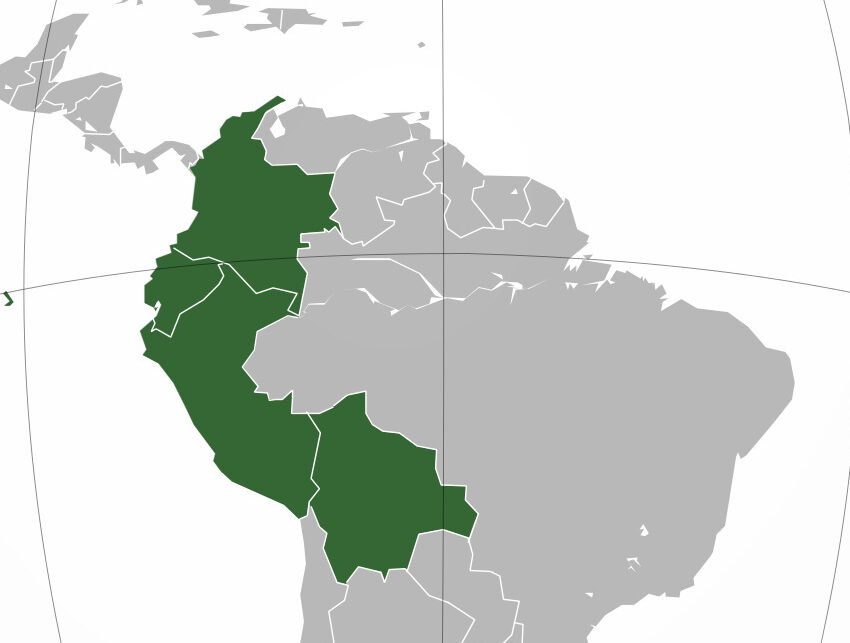
アンデス共同体(Comunidad Andina、CAN)は、南米4カ国で構成される貿易コンソーシアムである:コロンビア、ペルー、エクアドル、ボリビア。 1969年、カルタヘナ協定によって設立された。
CAN化粧品規制は、決定516「Armonización de Legislaciones en materia de Productos Cosméticos」に基づいており、2019年11月付けで決定833に置き換えられた(ただし、COVIDのため2021年3月1日まで延期)。
新規則は従来のものと類似しているが、例えば化粧品のカテゴリーにいくつかの変更を導入し、定義や概念の一部についてさらなる詳細を定めている。
CAN諸国では、化粧品とは「人体の表在部(表皮、毛髪および毛細血管系、爪、唇および外性器)、または歯および口腔粘膜に接触することを意図した物質または製剤であって、洗浄、香水、外観の修正または改善、保護、良好な状態の維持、体臭の是正を唯一の目的または主な目的とするもの」と定義されている。
「疾病の予防、治療、診断を目的とした物質や処方、または人体への摂取、吸入、注射、移植を目的とした製品」は、化粧品の範囲には含まれません。
また、化粧品は治療効果を謳うことができないことも重要である。
以下は、アンデス共同体の化粧品カテゴリー一覧である:
- 子供用化粧品
- 目元用化粧品
- 肌用化粧品
- 唇用化粧品
- トイレ・身体衛生用化粧品(アルコール70%未満のウェットティッシュ、抗菌ジェルを含む)
- デオドラント・制汗剤
- 毛髪用化粧品
- 爪用化粧品
- 香水製品
- 口腔衛生および歯科衛生用製品
- 髭剃り・髭剃り後用製品
- 日焼け、日焼け止め、セルフ・タンニング用製品
- 脱毛剤
- 肌を明るくする製品
- 皮膚に塗る防虫剤
- その他当局が定めるもの
すべての化粧品は、上市前にCAN当局に届け出なければならない。 この義務的届出(Notificación Sanitaria Obligatoria, NSO)は、最初の販売国の領域内に設置された責任者が行わなければならず、7年間有効である。
以下の情報を通知書に記載しなければならない:
1- 一般情報
- 法定代理人または代理人の氏名および代理権に関する書類
- 製造者及びNSO保持者の氏名及び住所
- 該当する場合、包装業者とコンディショナーの名前と住所
- 製品名、および必要に応じて化粧品グループ名と製品ブランド名
- コマーシャル・プレゼンテーション
- 化粧品フォーム(ガレニックフォーム)
- テクニカル・マネージャー名
- 加盟国が定める納税証明書
2- 技術情報
質的な配合による製品説明。 制限物質や活性物質については、定量的な申告が必要です。 製品にナノ材料が含まれている場合、国家当局は、これらの材料の化学的同一性とサイズを通知する必要があります。
- INCI成分リスト
- 最終製品の有機的および物理化学的仕様
- 微生物学的仕様
- 最終製品の利点、主張、美容効果を確認する研究
- ラベル
- 製品の使用説明書(該当する場合
- 一次および二次梱包材(該当する場合
- バッチ番号コード化システムの説明
成分に関する制限は決定書に明記されている。 アンデス共同体当局は以下の国際リストを参照している:
- 食品医薬品局による成分リスト
- パーソナルケア製品評議会による成分リスト
- コスメティクス・ヨーロッパの成分リスト
- EUの化粧品成分に関する指令と規則
共同体はまた、特定の食材をめぐるいくつかの対策を講じた:
– 決議1905「アンディナ共同体における化粧品成分としての長鎖パラベンの使用を禁止する。
– 決議1953「石鹸に含まれる抗菌・防臭成分の使用制限と禁止」は、石鹸に含まれる抗菌成分の一部を禁止するものである。 また、他の化粧品に含まれるトリクロサンやトリクロカルバンも制限されている。
欧州共同体で適用される微生物学的限界値は、決議2120「化粧品製品微生物学的規格に関する欧州連合決議(Reglamento Técnico Andino sobre Especificaciones Técnicas Microbiológicas de Productos Cosméticos)」で規定されており、2021年3月1日にも適用される。
| 製品タイプ | 許容限界 |
| – 小児用製品(3 歳まで) – 目の周囲に使用することを意図した製品 – 粘膜に接触する製品 |
a) 好気性好中性微生物総数の最大限度: 5 x 102 UFC/g または mL b) 1 g または mL 中の緑膿菌の不在 c) 1 g または mL 中の黄色ブドウ球菌の不在 d) 1 g または mL 中の大腸菌の不在 |
| 微生物汚染の影響を受けやすいその他の化粧品 | a) 好気性中好気性微生物総数の上限: 5 x 103 UFC/g または mL b) 1 g または mL 中の緑膿菌の不在 c) 1 g または mL 中の黄色ブドウ球菌の不在 d) 1 g または mL 中の大腸菌の不在 |
| 外性器への使用を意図した製品 | この表に含まれる他の製品に指定された許容限界に加え、これらの製品は以下に準拠しなければならない:カンジダ・アルビカンスが存在しないこと。 |
ラベルについて、決定833号はアンデス技術規則に言及している。 しかし、今日現在、この規則はまだ存在せず、決定516号が適用されている。
決定516号によれば、ラベルには以下の情報を記載しなければならない:
- メーカー名または販売責任者名
- 製品の原産国
- 重量または体積の名目量
- 使用上の注意
- ロット番号
- 排出国のNSO番号
- INCIで表記された成分表の前に “Ingredients “と表記されているもの
ペルーでは、”Reglamento para el registro, control y vigilancia sanitaria de productos farmaceuticos y afines “が化粧品に関するアンデス共同体決定を参照している。
エクアドルでは、”Resolución 15 284-A “が “Reglamento Técnico Ecuatoriano RTE INEN 093 (1R) Productos Cosméticos “を批准しており、これはDecision 516に基づいている。
どのように機能するのか?
BIORIUSは、化粧品ラベルに記載された必要な情報の確認と配合レビューを行います。
- フォーミュラレビュー:成分および不純物の毒性学的および規制上の評価、INCIリストおよび警告の設定。分析終了後、以下の要素を強調したフォーミュラ・レビュー・レポートが発行される:
- 原材料
- 各成分の割合
- 制限事項(決定833号、決議1905号および1953号より)
- 安全マージン
- INCIリスト
- 警告
- 戦略的提言を含む専門家のコメント
- 化粧品ラベルの必要情報の検証:決定516に基づく
BIORIUSは、これらの重要なステップを通じて、製品の上市に必要な化粧品登録ファイルの作成をサポートします。
お問い合わせ
アドバイス、お見積もり、ご質問への回答が必要ですか?お問い合わせ
こちらのフォームにご記入いただくか、info@biorius.com まで直接お問い合わせください!
Bioriusは、15年以上にわたる化粧品規制のスペシャリストとして、化粧品を様々な市場に投入するための信頼性の高いターンキーソリューションを提供しています:
- ヨーロッパ、イギリス、アメリカ、そして60カ国以上における化粧品規制の第一級スペシャリスト
- 50名の規制専門家、毒物学者、薬剤師、化学者がお客様にサービスを提供します。
- 最短の納期と高品質のサービスの両方を保証する独自のモデル。ご興味がおありですか?もっと詳しくお知りになりたい方はお問い合わせください!
- 隠れたコストはありません: ビオリアスは、ご質問、お電話、打ち合わせに一切費用をいただきません。
- クラス最高のITツールを無料でご利用いただけます。
- すでに1,500社以上の海外のお客様がビオリアスを選んでいます!
- 私たちは10万以上の製品を評価し、15年以上にわたって常にコンプライアンスを管理してきました。
Need to notify Biorius of an adverse effect related to the use of a cosmetic product for which Biorius’ name and address appear on the product labeling? Please complete THIS FORM, we will respond as soon as possible.
「*」は必須フィールドを示します